




| O projekcie | Do pobrania | Publikacje | Wykonawcy | Osiągnięcia |
| Aktualności |
|
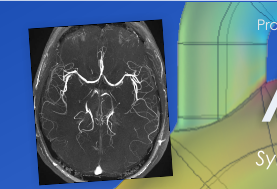
2.12.2015 - Nasz najnowszy artykuł o symulacji obrazowania Time-of-Flight oraz Phase Contrast Angiography jest już dostępny on-line. Zachęcamy do lektury.
30.11.2015 - W zakładce Do pobrania dodaliśmy odnośnik do projektu dla środowiska Xcode z naszą implementacją algorytmu do symulacji rozrostu drzew naczyń krwionośnych. Zachęcamy do pobierania :-). 6.10.2015 - Udostępniamy dwa nowe syntetyczne modele rozgałęzienia tętnicy szyjnej (zobacz). 15.08.2015 - Rozpoczynamy realizację nowego projektu nt. symulacji rezonansu magnetycznego. Tym razem zajmiemy się modelowaniem perfuzji nerek. Wkrótce pojawi się więcej informacji. |
| Polecamy |




|
| Licznik wizyt |
|
Liczba odsłon strony od 1.03.2015 r. |
Symulacja obrazowania magnetyczno-rezonansowego
Schemat zaprojektowanego symulatora przedstawiono na ryunku poniżej. Uwidocznione są w nim cztery podstawowe bloki funkcjonalne: cyfrowy fantom organu, moduł zarządzający sekwencją, jądro symulacji oraz blok rekonstrukcji obrazu.
Schemat blokowy systemu do symulacji MRI.
Cyfrowy fantom obrazowanego organu
Cyfrowy fantom obrazowanego organu składa się z geometrycznego modelu naczynia lub układu naczyń wypełnionego cząstkami zgodnie z metodą opisaną w sekcji Symulacja przepływu. Dodatkowo fantom może zawierać komponenty reprezentujące tkankę stałą otaczającą naczynia. Tkanka stała modelowana jest za pomocą wirtualnych cząstek podobnych do cząstek krwi. Cząstki tkanki stałej równomiernie wypełniając obszar wokół naczyń (rysynuek u dołu), przy czym w odróżnieniu od cząstek krwi, nie leżą na żadnych trajektoriach, a więc ich położenie jest niezmienne w czasie. Każdej cząstce – zarówno ruchomej, jak i stałej – odpowiada trójwymiarowy wektor magnetyzacji, który na początku symulacji inicjalizowany jest do stanu równowagi termicznej. Wektor ten podlega następnie różnym transformacjom zgodnie z przebiegiem sekwencji pomiarowej i zależnie od parametrów magnetycznych ośrodka, do którego należą (krwi lub tkanki stałej), czyli gęstości protonowej ρ i czasów relaksacji T1 i T2. Symulacja obrazowania dla poszczególnych komponentów organu wykonywana jest oddzielnie. Wyniki pomiarów są sumowane przed rekonstrukcją obrazu. Opcjonalnie, dla danego komponentu można także zdefiniować wartość przesunięcia chemicznego, odpowiedzialnego za błędne kodowanie przestrzenne spinów znajdujących się na granicy wody i tkanki tłuszczowej.
Rozkład cząstek tkanki otaczającej naczynia (kolor niebieski).
Sekwencja obrazowania
Moduł zarządzający sekwencją wywołuje w określonych krokach czasowych symulacji jedną z czterech głównych procedur odwzorowujących numerycznie: 1) pobudzenie cząstek impulsem RF, 2) swobodną precesję, 3) precesję przy włączonych gradientach pola magnetycznego oraz 4) próbkowanie sygnału. Sekwencja wymienionych zdarzeń powtarzana jest zgodnie z zadanymi parametrami: TR – czas repetycji (pomiędzy kolejnymi impulsami pobudzającymi) oraz TE – czas echa (pomiędzy pobudzeniem a środkiem okna akwizycji sygnału). W obrazowaniu magnetyczno-rezonansowym wyróżnia się dwie podstawowe sekwencje pomiarowe – echa spinowego (SE) oraz echa gradientowego. Zaprojektowany symulator implementuje obydwa typy sekwencji, jednakże w przypadku sekwencji angiograficznych (zarówno ToF, PCA, jak i SWI) stosowana jest tylko sekwencja GE. Dodatkowym parametrem w sekwencji GE jest kąt odchylenia (ang. flip angle, FA) wektora magnetyzacji od kierunku głównego pola magnetycznego tomografu B0, określający wielkość pobudzenia spinów, czyli długość rzutu wektora magnetyzacji na płaszczyznę poprzeczną do B0. Moduł zarządzający obejmuje także pełną definicję protokołu pomiarowego wraz z zaimplementowanymi opcjami skanowania, takimi jak
- kompensacja przepływu (redukcja artefaktów powstałych w wyniku dużej różnicy prękości spinów w obrębie jednego woksela obrazu),
- pobudzenie o zmiennym kącie odchylenia (ang. ramped pulse – technika stosowana w obrazowaniu 3D ToF dla zapobiegania zbyt szybkiemu nasyceniu spinów przepływających przez szeroką warstwę obrazowania),
- podział trójwymiarowego obszaru obrazowania na tzw. sztaby o mniejszej grubości (ang. Multiple Overlapped Thin Slab Acquisition, MOTSA; również zapobiegający nasyceniu spinów).
Obliczanie sygnału
Obliczenia wykonywane w jądrze symulacji bazują na równaniu Blocha, które stanowi klasyczny opis zjawiska NMR. Równanie to posiada rozwiązanie analityczne definiujące stan wektora magnetyzacji $\mathrm{\textbf{M}}$ cząstki $p$ w chwili $t$ w zależności od stanu w kroku poprzednim ($t-\Delta t$) jako
$$\mathrm{\textbf{M}}_p(t) = Rot_z(\theta_g)Rot_z(\theta_i)R_{\mathrm{relax}}R_{\mathrm{RF}}\mathrm{\textbf{M}}_p(t-\Delta t),$$ gdzie operator $Rot_z(\theta_g)$ odpowiada gradientowi kodowania fazy, $Rot_z(\theta_i)$ powoduje obrót wektora magnetyzacji w wyniku niejednorodności pola magnetycznego, $R_{\mathrm{relax}}$ uwzględnia zjawiska relaksacji wzdłużnej i poprzecznej, człon $R_{\mathrm{RF}}$ jest natomiast odpowiedzialny za obrót wektora magnetyzacji wokół osi y (pobudzenie). Należy zwrócić uwagę, że prawidłowe wyznaczenie nowego stanu wektora magnetyzacji wymaga określenia położenia cząstki względem środka gradientu. W przypadku poruszających się cząstek, stan wektora $\mathrm{\textbf{M}}_p$ należy aktualizować w odstępach czasowych pozwalających zachować precyzję zarówno symulacji przepływu, jak i zjawiska rezonansu magnetycznego. W wykonanych eksperymentach, krok ten ustala się zgodnie z interwałem czasowym dla próbkowania sygnału. Sama operacja próbkowania w obrębie jednej repetycji polega natomiast na sumowaniu wektorów magnetyzacji poprzecznej wszystkich cząstek w $N_x$ krokach czasowych, zgodnie z równaniem $$s(t) = \sum_{p=1}^{n_p}\vec M_p(t)\vec x + j\sum_{p=1}^{n_p}\vec M_p(t)\vec y,$$ gdzie $N_x$ oznacza liczbę wokseli obrazu w kierunku kodowania częstotliwości, zaś $n_p$ – liczbę cząstek. W ten sposób wypełniany jest jeden rząd w tzw. zespolona przestrzeni danych k-space. Częstotliwość próbkowania stanowi zatem iloraz liczby punktów próbkowania $N_x$ oraz długości okna akwizycji. Kolejne rzędy wypełniane są w $N_y$ oraz – w przypadku obrazów 3D – $N_z$ krokach kodowania fazy, przy czym każdy krok kodowania fazowego odbywa się w oddzielnych repetycjach sekwencji pomiarowej.
Rekonstrukcja obrazu
Zmierzona przestrzeń k-space podlega następnie odwrotnej transformacji Fouriera, co prowadzi do rekonstrukcji obrazu. Przed rekonstrukcją możliwe jest dodanie do zmierzonego sygnału szumu modelowanego za pomocą rozkładu normalnego o zadanej wartości odchylenia standardowego σ. Moduł rekonstrukcji obrazu został zaimplementowany w środowisku Matlab.

